Dnešní článek o kardiologických metodách napsala moje kamarádka Ing. Michaela Šromová, která se zabývá katétrovou ablací a spolupracuje přímo na sále s lékaři při výkonech jako klinický inženýr. Míšu jsem proto pořádala o úvodní článek do této ještě stále poměrně nové metody a doufám, že se vám bude líbít a že to není poslední Míšin příspěvek zde :-).
Jako vždy otázky směřujte do zpráv kardioblogu nebo na email janepear@email.cz, otázky přímo na míšu také tam.
Katétrová radiofrekvenční (RF) ablace arytmií
Katetrizační ablace srdečních arytmií je metoda, při které se do určitého místa v srdci, které je zodpovědné za vznik či šíření tachykardie, aplikuje pomocí katétru energie, která vytvoří v daném místě lézi. Tento výkon probíhá na katetrizačním sále. Ablační generátor generuje RF energii na hrot ablačního katétru. Přes ablační katétr se aplikuje střídavý nemodulovaný vysokofrekvenční proud o frekvenci 500-1000 kHz.
Elektrická energie proudí mezi hrotem katétru a velkoplošnou indiferentní elektrodou, která je umístěna na zádech pacienta. Při průchodu RF proudu se místo dotyku ablačního katétru s tkání zahřívá a dochází k tvorbě léze. Vytvořena jizva není vodivá. Ablační katétry lze z hlediska konstrukce rozdělit na nechlazené a na katétry chlazené fyziologickým roztokem. U katétrů chlazených se tvoří větší a hlubší léze v důsledku aplikace vyšší energie.
Léčebný postup při katetrizační ablaci je ovlivňován mechanismem tachykardie, přítomností strukturálního postižení srdce, lokalizací a rozsahem klíčového místa tachykardie. [1, 2, 3, 4, 5, 6]
Rizika katetrizační ablace arytmií
Jako každý invazivní výkon má i katetrizační ablace tachykardií svá rizika, mezi které patří tromboembolické komplikace, poškození převodního systému, poranění cév v místě vstupů katétrů do těla pacienta (obvykle třísla). Při ablaci může dojít také ke vzniku reaktivního perikardiálního výpotku nebo tamponády srdeční. Některé z těchto komplikací vyžadují urgentní řešení. [1, 4]
Indikace ke katetrizační ablaci
Katetrizační ablace je nefarmakologická metoda léčby tachykardií. Indikace je poměrně jednoznačná u typické AVNRT, WPW syndromu a typického flutteru síní.
U fibrilace síní bývá ablace indikována až po selhání antiarytmické léčby.Při záchytu symptomatické fibrilace síní u mladého člověka by však měla být RF ablace metodou první volby.
U pacientů s implantovaným kardioverter-defibrilátorem je ablace indikována v případě opakovaných výbojů nebo v případě recidivujících komorových arytmií.
U pacientů s idiopatickými tachykardiemi je ablace indikována při symptomatologii. [2, 4, 5]
Průběh katetrizační ablace
Většina výkonů se provádí endokardiálně (na obrázku 1 je uvedeno zavádění katétru), tj. katétry jsou do srdce vedeny cévním řečištěm, další možností je epikardiální či chirurgický přístup.
Na začátku výkonu pokud není arytmie jednoznačně dokumentovaná a nebo není jasně známý mechanismus je nutné před vlastním výkonem provést elektrofyziologické vyšetření (EFV). Pomocí intrakardiálního EKG je arytmie zmapována a posléze je aplikována RF energie. Méně složité výkony jako je AVNRT, WPW syndrom, typický flutter síní jsou mapovány pouze s využitím intrakardiálního EKG a za RTG kontroly. V případě komplexních arytmií se využívají 3D elektroanatomické mapovací systémy – například CARTO 3, CARTO XP, EnSite NavX, EnSite Velocity (viz obrázek 2).
Některá pracoviště používají také magnetické či robotické naváděcí systémy. Na robotických systémech se v dnešní době dělají hlavně ablace fibrilace síní. Magnetický navigační systém je vhodný převážně pro řešení komorových tachykardií, složitých fokálních síňových tachykardií, případně k epikardiálnímu mapování. Největší výhodou těchto systémů je stabilnější přítlak hrotu ablačního katétru k myokardu, díky čemuž se tvoří dokonalejší léze.
Délka výkonu se u různých druhů tachykardií liší. Délka RF ablace jednodušších arytmií, jako je AVNRT či typický flutter síní, bývá okolo 1 hodiny. Komplexní arytmie, jako je fibrilace síní, fokální síňová tachykardie či komorové tachykardie, mohou trvat od 3 až do 10 hodin.
Po ukončení RF ablace a normalizaci srážlivosti krve se pacientovi vytáhnou z cév katétry a jejich zavaděče a na místo vstupu do žíly či tepny se přiloží zátěž, aby pacient nekrvácel. Zátěž bývá přiložena po dobu 6-12 hodin, délka přiložení zátěže se liší například podle délky ablace nebo podle toho, zda byly katétry zaváděny žílou či tepnou. [2, 4, 5]
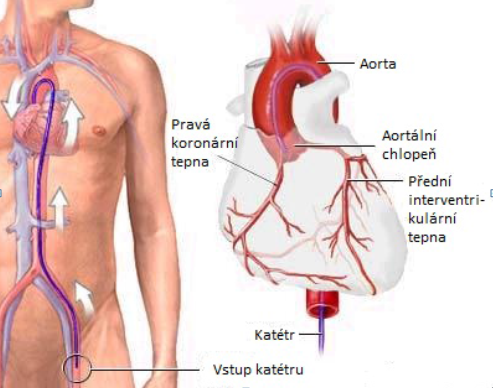 |
| Obrázek 1: Způsob zavedení katétru endokardiálním přístupem |
 |
| Obrázek 2: Ovladovna – na levých monitorech je zobrazeno intrakardiální EKG, na pravém monitoru mapovací systém EnSite Velocity a v pozadí elektrofyziologický sál |
Radiofrekvenční ablace fibrilace síní
Při RFA fibrilaci síní se zavádí 3 katétry. Diagnostický dekapolární CS katétr je zaveden z pravé síně do koronárního sinu, zde snímá jak aktivaci síní, tak komor a během používání mapovacího systému slouží také jako reference.
Kvadrupolární ablační katétr a duodekapolární cirkulární Lasso katétr je nutné zavést do levé srdeční síně, není-li přítomno PFO (foramen ovale patens), pak je nutné provést tzv. dvojitou transseptální punkci, jelikož se jedná o levosíňovou arytmii, která je nejčastěji spouštěna ektopickou aktivitou z plicních žil. U levosíňových výkonů je nutné pacienta heparinizovat. Používají se jak intraventrikulární bolusové dávky heparinu, tak kontinuální proplach transseptálních sheatů heparinizonovaným fyziologickým roztokem, přičemž při ablaci se rychlost proplachu ablačního katétru zvyšuje.
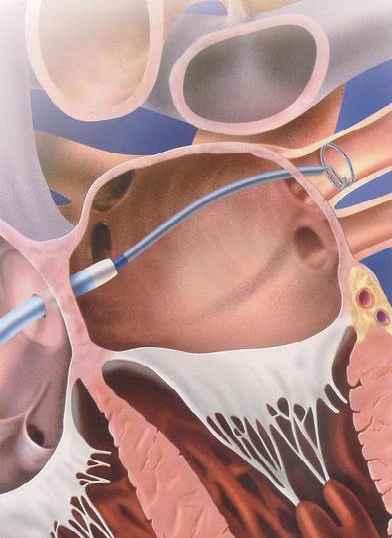 |
| LASSO katétr v ústí plicních žil |
Během výkonu se opakovaně v pravidelných intervalech vyhodnocuje ACT čiAPTT a podle výsledku je heparinizace upravována. Po zavedení katétrů i do levé síně se přistupuje k tvorbě anatomické mapy pomocí mapovacího systému (viz obrázek 2). Následně se již přistupuje k samotné ablaci, která spočívá, u paroxyzmální formy fibrilace síní, pouze v odizolování plicních žil. Cirkulární Lasso katétr se postupně zavádí do všech plicních žil a ablačním katétrem se postupně vytváří cirkulární léze v ústí plicních žil. Cílem je dosáhnout elektrické izolace všech plicních žil. Na obrázku 3 a 4 si lze všimnout rozdílu mezi neizolovanou a izolovanou plicní žilou. Jedná-li se o perzistující formu fibrilace síní, pak je nutné k cirkulárním lézím obkružujícím plicní žíly doplnit ještě léze lineární. Nejčastěji na stropě levé síně (tato lineární léze spojuje cirkulární lézi obkružující levé plicní žíly s cirkulární lézí obkružující pravé plicní žíly), dále na mitrálním isthmu a epikardiálně v koronárním sinu.
Před přistoupením k ablaci v koronálním sinu se kontroluje, zda nedošlo k rekondukci vedení ve vytvořených lézích. Následně po vytvoření poslední lineární léze v koronárním sinu je výkon ukončen. Nedojde-li u perzistující formy fibrilace síní během ablačního výkonu k indukci sinusového rytmu, je sinusový rytmus následně obnoven pomocí elektrické kardioverze.
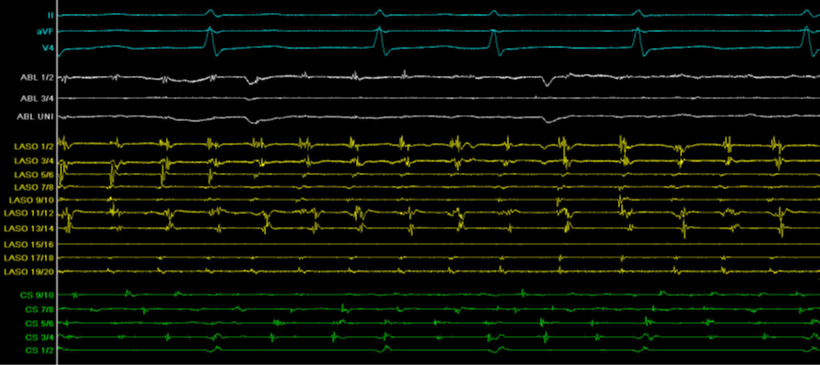 |
| Obrázek 3: Ukázka fibrilace síní na intrakardiálním EKG (Lasso zavedeno v plicní žíle, která zatím není izolována) |
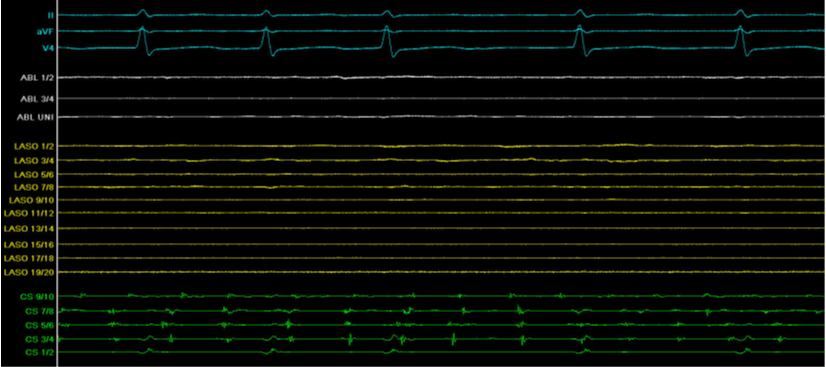 |
|
Obrázek 4: Ukázka izolované plicní žíly na intrakardiálním EKG
(v CS katétru fibrilace síní, v Lasso katétru průkaz izolované plicní žíly) |
[1] Doporučené postupy pro diagnostiku a léčbu supraventrikulárních tachyarytmií [online]. [cit. 2011-04-03]. Dostupné z: http://www.kardio-cz.cz/resources/upload/data/23_31-Guidelines-supraventrikularni_tachyarytmie.pdf
[2] SANQUIS – 2001/16 Léčba tachyarytmií radiofrekvenční ablací [online].[cit. 2010-12-02]. Dostupné z: http://www.sanquis.cz/index1.php?linkID=art889
[3] ASCHERMANN, Michael: Kardiologie. Galén, Praha, 2004, ISBN 80-7262-290-0.
[4] ŠROMOVÁ, Michaela: Hodnocení srdečních arytmií. Brno: Vysoké učení technické v Brně, Fakulta elektrotechniky a komunikačních technologií, 2011, 64 s., 1 příl. Vedoucí bakalářské práce prof. Ing. Ivo Provazník, Ph.D..
[5] SCHMITT, Claus, Isabel DEISENHOFER, Bernhard ZRENNER: Catheter Ablation of Cardiac Arrhythmias. Steinkopff Verlag, Darmstadt, 2006, ISBN 3-7985-1575-1.
[6] STÁREK, Zdeněk, Martin EISENBERGER, Libor ZAORAL, Pavel LEINVEBER, Miroslav NOVÁK: Radiofrekvenční katetrizační ablace supraventrikulárních arytmií, historie a současnost. Solen – Intervenèní a akutní kardiologie; číslo 5, 2006.

